Introduction du dépistage primaire du papillomavirus à partir du 1.1.2025

- Dépistage
- Suivi diagnostique ou thérapeutique
À partir du 1er janvier prochain, la nomenclature INAMI pour les examens cytologiques et le PCR HPV ADN effectué dans le cadre du cancer du col de l’utérus sera radicalement modifiée.
La nouvelle nomenclature différencie sur la base des classes d’âge et prévoit en outre un remboursement en fonction des indications clinico-diagnostiques et pour les populations à haut risque. Le test combiné (PCR HPV ADN avec cytologie primaire et cytologie avec PCR HPV ADN primaire) ainsi que le testing en général en dehors de ce dépistage régulier sont à la charge de la patiente.
DANS LE CADRE D'UN DÉPISTAGE
Dans le cadre du dépistage (où les tests réflexes sont automatiquement ajoutés le cas échéant) :
- <25 ans : pas de remboursement.
- 25-29 ans : cytologie primaire et PCR HPV ADN comme test réflexe sur le même prélèvement en cas de présence démontrée de cellules atypiques (ASC-US, …). La périodicité est d’une fois toutes les 3 années civiles, par analogie avec la pratique actuelle.
- 30-64 ans : PCR HPV ADN primaire, suivi d’une cytologie comme test réflexe sur le même échantillon si le test HPV est positif ou non concluant. Cela avec une périodicité de tous les 5 ans.
- >64 ans : aucune intervention, sauf si aucun test de dépistage du cancer du col de l’utérus n’a été remboursé au cours des 10 années civiles précédentes. Si cette condition est remplie, la patiente a droit à un test combiné composé d’une cytologie et d’un PCR HPV ADN.
Il convient de noter ici la définition de l’âge utilisée : on attribue à la patiente l’âge qu’elle atteindra le 1er janvier de l’année.
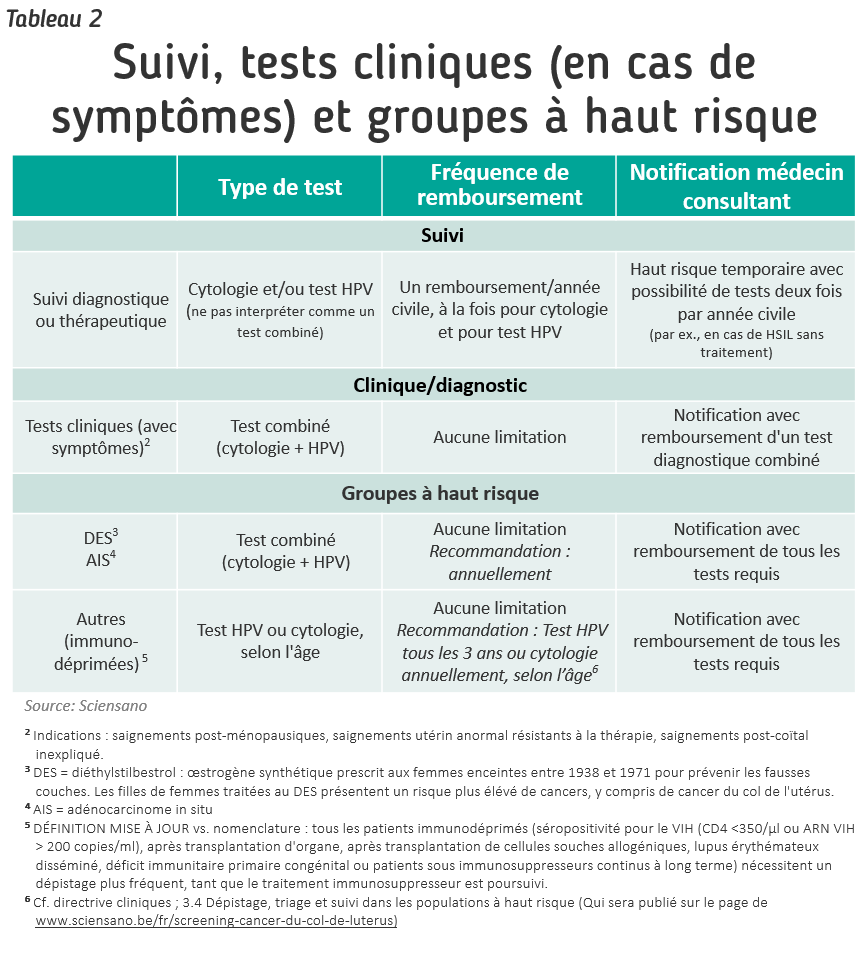
SUIVI DIAGNOSTIQUE OU THÉRAPIQUE
Dans le cadre d’un suivi diagnostique ou thérapeutique (voir tableau 1 : 2ème triage – répétition du test), l’INAMI prévoit une intervention pour le PCR HPV ADN ou la cytologie une fois par année civile pour autant que le suivi soit médicalement nécessaire selon les lignes directrices publiées par Sciensano.
En cas de nécessité médicale, cette fréquence peut être augmentée à deux fois par année civile. Un formulaire de notification standardisé est requis pour cette nécessité médicale (disponible via INAMI).
Ce formulaire doit être remis par le médecin demandeur au médecin-conseil de l’institution d’assurance du bénéficiaire, avec la mention « risque temporaire élevé ». Il est recommandé de mentionner également l’indication retenue dans le formulaire de demande. Cette notification reste en vigueur aussi longtemps qu’une fréquence de suivi accrue est médicalement nécessaire.
Si les patientes ont droit à un suivi diagnostique ou thérapeutique, nous le mentionnerons comme conseil dans le rapport.
INDICATIONS CLINIQUES ET DIAGNOSTIQUES
Pour les indications suivantes, 1 test combiné diagnostique (cytologie + PCR HPV ADN) sera remboursé :
- Perte de sang post-ménopause
- Perte de sang utérine anormale résistante au traitement
- Perte de sang postcoïtale inexpliquée
Un formulaire de notification standardisé est applicable, mentionnant l’indication.
POPULATIONS À HAUT RISQUE
Dans les populations à haut risque, il n’y a pas de restriction de fréquence concernant le test combiné diagnostique (cytologie + HPV PCR-DNA), en fonction de la nécessité médicale. Un formulaire de notification standardisé mentionnant l’indication est également d’application.
- Patients immunodéprimés :
- Personnes séropositives
- Après une transplantation d’organe
- Après une transplantation de cellules souches allogènes
- Lupus érythémateux disséminé
- Déficit immunitaire primaire congénital
- Traitement immunosuppresseur pour :
- Maladies inflammatoires de l’intestin
- Troubles rhumatologiques
- Sarcoïdose
- Neuromyélite optique
- Victimes de l’exposition au DES
- Adénocarcinome in situ
Des informations plus détaillées sont disponibles sur le site d’INAMI, y compris les algorithmes de tests suivants:
[Cliquez sur l’image pour l’agrandir]
Les tests utilisés par le laboratoire sont homologués par le gouvernement et accrédités ISO 15189. Les résultats sont systématiquement enregistrés de manière conforme auprès de l’organisme compétent : le Registre belge du cancer.
Si vous faites les demandes sur papier, vous recevrez les formulaires de demande appropriés avant la fin de l’année. Une version numérique sera également disponible pour ceux qui prescrivent par voie électronique. Cela devrait vous permettre de préciser suffisamment les indications clinico-diagnostiques, ce qui est important car c’est sur cette base que sera décidé le parcours de l’échantillon dans le laboratoire, ce qui détermine également la tarification.
Enfin, nous tenons à préciser qu’il n’y a pas de changement en termes d’échantillonnage : le Cervex-Brush et le récipient ThinPrep restent le matériel privilégié.
Si vous avez des questions, n’hésitez pas à nous contacter.